Introducción
Los trastornos funcionales y motores digestivos comprenden un amplio grupo de patologías que pueden afectar a cualquier tramo del tracto digestivo. La causa de los trastornos motores y funcionales es desconocida, pero sabemos que los pacientes que los sufren pueden presentar alteraciones a cualquier nivel del eje cerebrointestinal. En algunos casos, como el reflujo gastroesofágico o la acalasia, la alteración es sobre todo motora, en el esófago y la unión esofagogástrica.
En otros casos, como en el síndrome del intestino irritable o la dispepsia funcional, la alteración parece más difusa, ya que se puede afectar desde la transmisión de los impulsos en el sistema periférico, hasta su interpretación en el sistema central. Así, se sabe que los factores periféricos, como la inflamación o la infección, y los factores centrales, como el estrés o los episodios de la vida cotidiana, tienen una influencia en el desarrollo de estos trastornos.
Debido a la complejidad de los trastornos funcionales digestivos, las potenciales dianas terapéuticas para su tratamiento son también muy variadas. A lo largo de los años se han desarrollado diversos fármacos para el tratamiento de estos trastornos, como los procinéticos y los antiespasmódicos, o fármacos que cambian el entorno intraluminal, como los antisecretores o los probióticos. Sin embargo, muchos de los tratamientos desarrollados han sido retirados del mercado, o no han llegado a comercializarse debido a los efectos secundarios que producían. En este trabajo vamos a comentar en detalle los nuevos tratamientos que se han desarrollado para los trastornos funcionales y motores digestivos, haciendo especial hincapié en los datos de que disponemos sobre su eficacia y seguridad.
 Novedades en el reflujo gastroesofágico
Novedades en el reflujo gastroesofágico
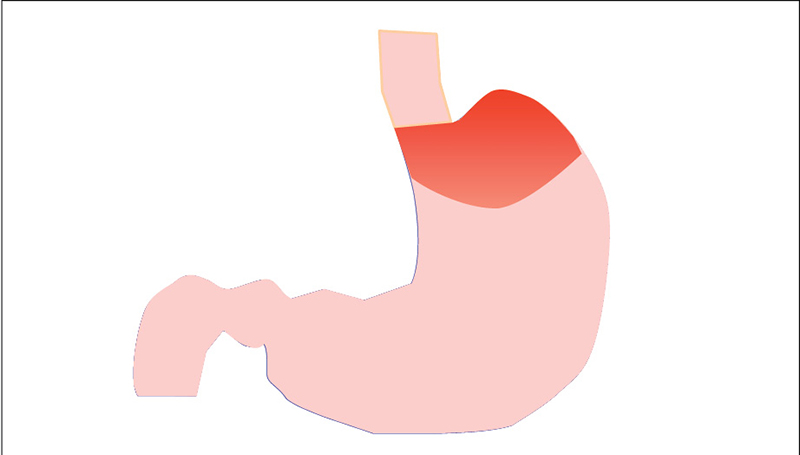
El tratamiento principal del reflujo gastroesofágico sigue siendo la supresión de la acidez gástrica con fármacos antisecretores. Sin embargo, se sabe que aproximadamente el 30% de los pacientes con síntomas de reflujo no presenta una respuesta satisfactoria al tratamiento. Para estos pacientes se han desarrollado fármacos agonistas GABA, que inhiben la relajación transitoria del esfínter esofágico inferior. Sin embargo, el único fármaco de este tipo disponible en el mercado español es el baclofeno, que presenta numerosos efectos secundarios que dificultan su uso. En los últimos años se han generado nuevos conocimientos sobre un mecanismo hasta ahora desconocido como productor del reflujo, la cámara ácida (acid pocket) que se produce en la parte superior del estómago después de la ingesta (figura 1), y se han desarrollado tratamientos específicos, algunos de los cuales se han comercializado recientemente en España.
«Acid pocket», o cámara ácida posprandial
En condiciones basales, el contenido del estómago es ácido, con un pH muy bajo, alrededor de 1, debido a la secreción de ácido clorhídrico. Durante la ingesta, los alimentos se mezclan con las secreciones gástricas y se produce un efecto buffer que neutraliza parcialmente la acidez del estómago. Llama la atención que en muchos pacientes un gran número de los episodios de reflujo se producen durante el periodo posprandial, cuando en teoría no hay ácido en el estómago. Algunos estudios realizados en Escocia, mediante una retirada paulatina de un sensor de pH, introducido en el estómago durante el periodo posprandial, han puesto de manifiesto que en la parte superior del estómago se crea una pequeña cámara ácida, relacionada con el reflujo posprandial. Así, la distancia entre la cámara ácida y el epitelio escamoso esofágico es menor en los pacientes con reflujo gastroesofágico que en los controles, y la longitud de la cámara ácida es igualmente mayor en los pacientes. Asimismo, la posición de la cámara ácida está mucho más próxima al epitelio escamoso del esófago en sujetos con hernia de hiato de gran tamaño.
Tratamiento del «acid pocket»
La finalidad del tratamiento es aumentar la distancia que existe entre la cámara ácida del estómago y el epitelio escamoso esofágico. El desplazamiento de la cámara ácida hacia zonas más caudales puede conseguirse mediante alginatos, que son sustancias que crean una barrera física sobre dicha cámara, o mediante procinéticos, que favorecen el desplazamiento caudal de la cámara al facilitar el vaciamiento gástrico.
Alginatos
Los alginatos son sustancias que se obtienen de unas algas marinas que se encuentran en el Mar del Norte. Estas sustancias reaccionan con el ácido del estómago formando una capa gelatinosa y espesa. En España está comercializado Gaviscon®, que es una mezcla de alginato, bicarbonato sódico y carbonato de calcio. La misión del bicarbonato sódico es reaccionar con el ácido formando CO2, que se mezcla con el alginato y lo hace flotar sobre la superficie gástrica. La función del carbonato de calcio es dar consistencia al alginato. Como resultado de estas reacciones locales en el estómago, se forma una especie de balsa que flota encima del contenido gástrico, que actúa a modo de tapón e impide el reflujo gastroesofágico. Esta mezcla con alginato ha demostrado desplazar lejos de la unión esofagogástrica la cámara ácida posprandial, y reducir el reflujo gastroesofágico en el periodo posprandial1.
Una de las ventajas que ofrecen los alginatos es que actúan de forma local intraluminal, no se absorben y no se metabolizan en el organismo, lo que les confiere un alto nivel de seguridad. Carecen de efectos sistémicos, y no interaccionan con las vías metabólicas de otros medicamentos, por lo que pueden administrarse en mujeres embarazadas y pacientes polimedicados, y combinarse con los inhibidores de la bomba de protones (IBP). Algunos estudios recientes han demostrado que en los pacientes que no responden adecuadamente a los IBP, la adición de alginato a estos fármacos produce una mejoría en una proporción significativamente mayor de pacientes, por lo que esta combinación podría ser recomendable en estos casos. Si bien lo lógico es pensar que el alginato ha de impedir todo tipo de reflujo, tanto ácido como no ácido, hasta hoy no existe ningún estudio controlado que valore específicamente este aspecto.
Procinéticos
Los fármacos procinéticos comercializados en España son básicamente agonistas de la 5-HT4, como la cinitaprida o la prucaloprida, antiheméticos, como la metoclopramida, la cleboprida y la domperidona, y fármacos con un mecanismo dual de acción, como la levosulpirida. A día de hoy, no se dispone de ningún estudio que valore la acción de ninguno de estos fármacos sobre la cámara ácida posprandial, por lo que su posible beneficio sobre ésta se desconoce. La azitromicina es un antibiótico macrólido similar a la eritromicina, que tiene una potente acción procinética, ya que actúa como agonista de la motilina. Recientes estudios han mostrado que la azitromicina es capaz de desplazar la cámara ácida posprandial (acid pocket) hacia zonas más distales del estómago, alejadas de la zona de transición de los epitelios esofágico y gástrico, y esto se asocia a un cambio en las características del reflujo, reduciéndose exclusivamente el reflujo gastroesofágico de tipo ácido. Sin embargo, la azitromicina es un antibiótico, por lo que su uso generalizado en el tratamiento del reflujo no puede recomendarse; por tanto, estos estudios han de considerarse como una prueba de concepto del efecto de los procinéticos sobre la cámara ácida posprandial. Sin embargo, la potencia y el mecanismo de acción de la azitromicina no es la misma que la de otros fármacos procinéticos comercializados en España, por lo que serían necesarios más estudios específicos para conocer si éstos también poseen un efecto similar al de los agonistas de la motilina.
Novedades terapéuticas del síndrome del intestino irritable y otros trastornos funcionales digestivos
El síndrome del intestino irritable es el trastorno funcional digestivo más conocido y posiblemente más complejo. Se trata de un trastorno multifactorial, por lo que las posibles dianas terapéuticas de este trastorno son múltiples. Por otro lado, existen diferentes síntomas que se producen de forma crónica pero que no llegan a cumplir los criterios del síndrome del intestino irritable, y conforman otros trastornos funcionales digestivos. En estos últimos años se han comercializado en España diversos fármacos y complementos alimentarios de origen natural para el tratamiento de estos trastornos. Paralelamente, se han desarrollado dietas específicas que podrían ayudar al tratamiento de estos pacientes. Pero quizá la novedad principal es que en 2012 la Agencia Europea del Medicamento (EMA) aprobó por primera vez un fármaco con la indicación específica de tratamiento del síndrome del intestino irritable, la linaclotida, que desde el año 2014 ya está disponible en España.
 Linaclotida
Linaclotida
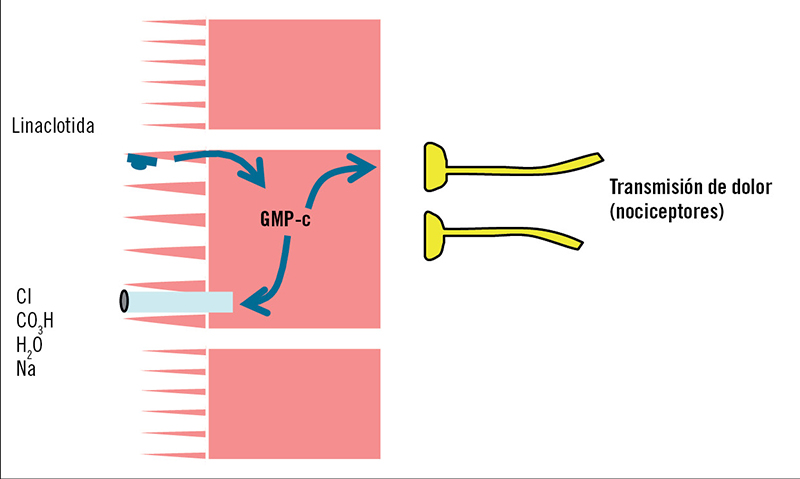
La linaclotida es un péptido sintético que actúa estimulando los receptores del subtipo C de la guanilato ciclasa (GC-C), situados en la superficie luminal del epitelio intestinal. La activación de CG-C produce un incremento en los niveles de guanosín monofosfato cíclico (GMPc), tanto intracelular como extracelular. El incremento de GMPc intracelular activa el regulador de la conductancia transmembrana de la fibrosis quística, que a su vez estimula la secreción de cloro y bicarbonato hacia la luz intestinal. El incremento extracelular del GMPc en el espacio basolateral actúa incrementando el umbral sensorial de la neuronas nociceptivas del colon, que son las productoras del dolor visceral a este nivel. El resultado final de estas dos acciones es, por un lado, el incremento de la secreción intraluminal y el tránsito intestinal, beneficiosos para tratar el estreñimiento, y por otro lado el aumento del umbral sensorial del colon, que permite actuar sobre el dolor visceral (figura 2). Los ensayos clínicos controlados en fase 3 realizados con linaclotida han incluido más de 1.600 pacientes de numerosos centros de Estados Unidos y Canadá con síndrome del intestino irritable y predominio de estreñimiento (SII-C), y han demostrado una eficacia superior del tratamiento con linaclotida respecto a placebo en todos los criterios de respuesta exigidos por la Food and Drug Administration (dolor abdominal e incremento de deposiciones espontáneas completas) y la Agencia Europea del Medicamento (EMA) (dolor y molestia abdominal, y alivio sintomático), así como en todos los síntomas secundarios de IBS-C evaluados2-4.
Además, dado que la linaclotida ejerce su acción estimulando los receptores de la guanilato ciclasa (GC-C), situados en la superficie luminal del epitelio intestinal, no requiere ser absorbida para ejercer su efecto, y ha mostrado un excelente perfil de seguridad. Así, la frecuencia y el tipo de efectos adversos registrados en los diferentes ensayos ha sido muy similar en los grupos tratados con linaclotida y placebo, con excepción de la diarrea, que fue mucho más frecuente en el grupo tratado con linaclotida (el 20 frente al 3%). Sin embargo, la diarrea fue leve o moderada en la mayoría de los pacientes, más importante durante la primera semana de tratamiento, y sólo provocó la interrupción del tratamiento en el 5% de los casos. No se ha registrado ningún efecto adverso grave relacionado con la diarrea, y globalmente la frecuencia de efectos adversos graves en los diferentes ensayos ha sido mínima, similar al placebo, y en ningún caso relacionados con el tratamiento. Por todo ello, la linaclotida se presenta como un fármaco completamente novedoso, con un mecanismo de acción muy definido, que desde su comercialización ha abierto nuevas posibilidades terapéuticas hasta ahora inexistentes para estos pacientes.
STW5 (iberogast®)
Se trata de una combinación de 9 extractos vegetales, que normalmente sería considerado como un preparado de tipo homeopático, pero que ha sido comercializado en España como un producto farmacológico. La idea de este producto es que cada uno de los diferentes extractos vegetales tiene una acción específica sobre el tubo digestivo, por lo que esta combinación podría actuar simultáneamente sobre diferentes mecanismos involucrados en los síntomas funcionales digestivos. A diferencia de lo que ocurre con muchos preparados de este tipo, iberogast® viene avalado por varios estudios controlados que han demostrado una mayor eficacia que el placebo sobre ciertos trastornos, como la dispepsia funcional o el síndrome del intestino irritable5. Asimismo, se han realizado estudios mecanísticos que muestran que STW5 favorece la relajación del fundus del estómago e incrementa la actividad motora del antro gástrico, lo que puede ser un mecanismo favorecedor de los síntomas en los pacientes con dispepsia funcional y saciedad precoz o digestión pesada. Por último, cabe reseñar que este fármaco ha sido comercializado en países como Alemania desde hace más de 40 años, y ha mostrado un alto perfil de seguridad; sus efectos secundarios son principalmente reacciones de hipersensibilidad a alguno de los componentes.
Tratamientos dietéticos
Muchos pacientes con trastornos funcionales digestivos refieren que sus síntomas empeoran con las comidas. Por este motivo, se han utilizado diferentes dietas en estos pacientes, e incluso se han desarrollado diversos test de intolerancias alimentarias, aunque la gran mayoría de ellos sin una base científica sólida ni con resultados contrastados sobre su eficacia. Recientemente se ha desarrollado en Australia una dieta que consiste en la supresión de oligosacáridos fermentables, disacáridos, monosacáridos y polioles (FODMAP)6. Se trata de una dieta muy estricta, que en estudios controlados con dieta estándar ha mostrado una mejoría significativa de los síntomas digestivos. Tanto el dolor como la distensión abdominal y las flatulencias se redujeron de forma significativa durante el consumo de la dieta de exclusión, mientras que estos síntomas permanecieron inalterados en los pacientes con dieta normal. Curiosamente, el efecto beneficioso de esta dieta se ha observado tanto en pacientes con intestino irritable y predominio de estreñimiento como en los pacientes con predominio de diarrea, si bien un cambio en la consistencia y frecuencia de las deposiciones sólo se produjo en estos últimos. Uno de los posibles mecanismos por los que esta dieta podría actuar es la disminución en la producción de productos derivados de la fermentación de azúcares, como el gas hidrógeno y metano, o los ácidos grasos de cadena corta.
Sin embargo, la presencia de una malabsorción de hidratos de carbono parece no predecir la respuesta a la dieta, ya que se ha descrito un efecto beneficioso similar en los pacientes con y sin intolerancia a la fructosa. Igualmente, en los últimos años el mismo grupo de investigadores ha señalado que hay pacientes con síndrome del intestino irritable que responden a una dieta sin gluten sin que sufran una enfermedad celiaca, como lo demuestra la normalidad en los resultados de los estudios serológicos, genéticos y anatomopatológicos. Debido a la falta de un tratamiento eficaz para estos pacientes, la aparición de manipulaciones dietéticas realmente efectivas podría suponer una alternativa terapéutica interesante; no obstante, estas dietas son altamente restrictivas, y los estudios publicados al respecto sólo han valorado su efecto a corto plazo (3 semanas). No está claro si un tratamiento prolongado puede provocar déficits alimentarios que deben sustituirse, ni se conocen las posibles pautas y efectos de la reintroducción de los alimentos, por lo que consideramos que aún es pronto para hacer una recomendación general sobre este tipo de dietas que, en caso de administrarse, deberían estar estrictamente controladas por nutricionistas.
 Nuevos fármacos procinéticos
Nuevos fármacos procinéticos
Prucaloprida
La cisaprida ha sido el fármaco procinético más utilizado y del que tenemos mejor conocimiento. Este fármaco ejercía su acción procinética al activar los receptores tipo 4 de la serotonina (5-HT4), que a su vez estimulan la secreción de acetilcolina favoreciendo las vías estimuladoras de la actividad motora intestinal. Debido a que a nivel cardiológico también existen receptores 5-HT4, se produjeron algunos casos de arritmias graves en los pacientes tratados con cisaprida que llevaron a la retirada de este fármaco. Desde entonces se ha producido un hueco importante en las posibilidades de tratar a los pacientes con alteraciones de la motilidad digestiva, que en España ha sido relativamente cubierto con fármacos como la cinitaprida o la levosulpirida, cuyas principales indicaciones son los trastornos motores del tracto digestivo superior (dispepsia y reflujo). La prucaloprida se comercializó en España en 2012, y tiene todas las condiciones para poder ocupar el hueco dejado por la cisaprida. Se trata de un fármaco activador ultraselectivo de los receptores 5-HT4, por lo que su acción en dosis terapéuticas se ejerce exclusivamente sobre los receptores situados en el intestino, sin acción sobre los receptores cardiológicos de la serotonina, por lo que está exento de efectos cardiovasculares. En estudios en fase 2 y 3, la prucaloprida ha mostrado un excelente perfil de seguridad, sin alteraciones en el ritmo cardiaco ni en el periodo QT del electrocardiograma7. A diferencia de otros procinéticos comercializados en España, la prucaloprida tiene como indicación exclusiva el tratamiento del estreñimiento.
Este efecto viene avalado por estudios controlados en fase 3 sobre más de 1.800 pacientes tratados durante 12 semanas con 2 o 4 mg de prucaloprida. Estos estudios han revelado un efecto superior de este fármaco sobre placebo en el número de deposiciones espontáneas completas, el número de deposiciones espontáneas, los síntomas abdominales relacionados con el estreñimiento, y la calidad de vida. El efecto secundario más frecuente fue la cefalea (documentada en un 25% de los pacientes durante el primer día de tratamiento). Sin embargo, tras el primer día de tratamiento la incidencia de cefalea se redujo a un 12-13% de los pacientes. Otros efectos secundarios fueron las náuseas, la diarrea y el dolor abdominal. El problema principal del tratamiento con prucaloprida reside en su elevado precio. Por ello, no debe considerarse como un fármaco de primera línea en el tratamiento del estreñimiento. Las últimas guías terapéuticas europeas del estreñimiento consideran que la prucaloprida está indicada en los pacientes con estreñimiento que no han respondido a dos laxantes diferentes8.
Bibliografía
1. Rohof WO, Bennink RJ, Smout AJ, Thomas E, Boeckxstaens GE. An alginate-antacid formulation localizes to the Acid Pocket to reduce acid reflux in patients with gastroesophageal reflux disease. Clin Gastroenterol Hepatol. 2013; 11(12): 1.585-1.591.
2. Kahrilas PJ, Boeckxstaens G, Smout AJ. Management of the patient with incomplete response to PPI therapy. Best Pract Res Clin Gastroenterol. 2013; 27: 401-414.
3. Kahrilas PJ, McColl K, Fox M, O'Rourke L, Sifrim D, Smout AJ, Boeckxstaens G. The acid pocket: a target for treatment in reflux disease? Am J Gastroenterol. 2013; 108: 1.058-1.064.
4. Quigley EM, Tack J, Chey WD, Rao SS, Fortea J, Falques M, et al. Randomised clinical trials: linaclotide phase 3 studies in IBS-C: a prespecified further analysis based on European Medicines Agency-specified endpoints. Aliment Pharmacol Ther. 2013; 37: 49-61.
5. Rahimi R, Abdollahi M. Herbal medicines for the management of irritable bowel syndrome: a comprehensive review. World J Gastroenterol. 2012; 18: 589-600.
6. Halmos EP, Power VA, Shepherd SJ, Gibson PR, Muir JG. A diet low in FODMAPs reduces symptoms of irritable bowel syndrome. Gastroenterology. 2013; 146(1): 67-75.
7. Camilleri M, Kerstens R, Rykx A, Vandeplassche L. A placebo-controlled trial of prucalopride for severe chronic constipation. N Engl J Med. 2008; 358: 2.344-2.354.
8. Tack J, Muller-Lissner S, Stanghellini V, Boeckxstaens G, Kamm MA, Simren M, et al. Diagnosis and treatment of chronic constipation: a European perspective. Neurogastroenterol Motil. 2011; 23: 697-710.
|
A recordar • El reflujo ácido posprandial está relacionado con la formación de una cámara ácida en la parte superior del estómago (acid pocket), próxima a la zona de transición del epitelio esofagogástrico. • Un preparado con alginato ha sido comercializado recientemente en España, y ha demostrado desplazar la cámara ácida posprandial lejos de la unión esofagogástrica y mejorar el reflujo esofagogástrico. • En los últimos años se han desarrollado nuevos tratamientos para los trastornos funcionales digestivos, que incluyen tanto fármacos que actúan sobre la hipersensibilidad visceral de estos pacientes como sustancias de fitoterapia de reciente comercialización en España y nuevas dietas de exclusión que han mostrado resultados esperanzadores a corto plazo. • En 2012 se comercializó en España un fármaco procinético que está indicado exclusivamente en pacientes con estreñimiento y fracaso en el tratamiento con laxantes (prucaloprida), y la EMA aceptó el primer fármaco indicado exclusivamente para el síndrome del intestino irritable (linaclotida). |

