Fue Subba Raw, involucrado en los estudios del ácido fólico, quien diseñó los antifolatos a demanda de Farber. Raw ya había descubierto que los antifolatos interferían en el metabolismo del ácido fólico y que inhibían el crecimiento celular. La ametopterina, antimetabolito análogo del ácido fólico, actúa principalmente sobre la fase S del ciclo celular, siendo un agente citotóxico. Inhibe irreversiblemente la reacción que comprende el paso de ácido dihidrofólico a ácido tetrahidrofólico, uniéndose a la enzima que cataliza dicha reacción, la dihidrofolato-reductasa ácida. Debido a este mecanismo se inhibe la formación de ADN y ARN y por ello, consecuentemente, no se produce la mitosis celular.
Farber, al hacer el uso de los antifolatos, no obtuvo resultados inmediatos, pero sí a largo plazo: sus pacientes en cuestión de unos meses habían mejorado notablemente y la enfermedad había remitido aunque no curado. Este descubrimiento supuso el inicio de un nuevo camino hacia futuras investigaciones enfocadas al tratamiento de enfermedades malignas como la enfermedad de Hodgkin, linfoma no Hodgkin, linfoma cutáneo de células T, osteosarcomas, enfermedades autoinmunes como la psoriasis, neoplasias de cabeza y cuello y en casos de metástasis, pudiendo administrarse por vía intratecal en este último caso, si afecta al sistema nervioso central.
Además, se lleva utilizando más de 25 años como tratamiento de elección de la artritis reumatoide en adultos, siendo aprobado su uso en el año 1988 por la FDA. A diferencia de los anteriores, en este caso no se conoce el mecanismo de acción, aunque se estima que está relacionado con sus propiedades inmunosupresoras.
En este trabajo nos hemos centrado en un estudio realizado en pacientes con asma dependientes de esteroides, en el cual el metotrexato realizaría su labor como economizador de glucocorticoides, reduciendo en alta medida la dosis de ellos y con ello sus efectos secundarios. Su eficacia en este campo sigue sin estar clara, pero no deja de ser una aplicación novedosa e innovadora, como bien demuestran los estudios realizados al respecto, para los enfermos de asma.
En ocasiones anteriores ya se habían intentado utilizar otros fármacos como ahorradores de glucocorticoides, es el caso de las ciclosporinas o las sales de oro pero sus efectos secundarios limitan su uso.
Objetivo
El objetivo del estudio analizado es, por tanto, evaluar la eficacia a largo plazo de metotrexato a dosis semanales bajas en la disminución de la dosis de esteroides orales, su tolerancia, y el potencial efecto beneficioso de la disminución de la dosis de esteroides en el metabolismo óseo.
Metodología
En primer lugar realizamos una búsqueda en la base de datos PubMed, utilizando como palabras clave «Methotrexate AND Investigation», y acotando con los siguientes filtros «texto completo», «humanos» y «últimos 5 años». Obtuvimos 39 resultados.
Con el fin de reducir el número de artículos y especificar más la información realizamos una segunda búsqueda en PubMed. Utilizamos como palabras clave «Methotrexate AND Asthma» utilizando los mismos filtros que en la primera búsqueda. Obtuvimos finalmente 8 resultados, los cuales utilizamos para esta revisión.
Resultados y discusión
En primer lugar, los investigadores utilizaron determinados criterios de exclusión para elegir a los pacientes para el estudio. Se excluyeron del estudio pacientes con la creatinina sérica menor de 133 mmol/L; con neoplasia anterior; diabéticos insulinodependientes; pacientes con obesidad mórbida; alcohólicos o con antecedentes de enfermedad hepática crónica así como con las transaminasas elevadas; enfermos con úlcera péptica; enfermedad psiquiátrica previa o actual; enfermedad pulmonar intersticial; SIDA; nivel de hemoglobina, plaquetas o glóbulos blancos bajo y las pacientes embarazadas entre otros. Quedando finalmente un total de 46 pacientes.
El estudio fue aleatorio, doble ciego y controlado por placebo. De los 46 pacientes 23 de ellos fueron tratados con placebo y los 22 restantes con metotrexato a una dosis de 10 mg/semana. A ambos grupos se les administró conjuntamente ácido fólico, evitando efectos secundarios del metotrexato, con el fin de evidenciar tanto de cara al médico como a los pacientes cual pertenecía a cada grupo. Como los esteroides, se empleó la 6-metilprednisolona vía oral.
Primeramente, se realizó un estudio de aleatorización (sin incluir el metotrexato) en el cual las dosis de esteroides se iban estrechando progresivamente 2 mg/día cada dos semanas, hasta una disminución del FEV1 menor o igual al 5%. Cuando esto ocurría la dosis de esteroides se aumentó al nivel anterior y el proceso se repitió de nuevo. Se repitió de nuevo la prueba, y cuando la disminución de esteroides falló por tercera vez se determinó que se había alcanzado la dosis mínima de esteroides requerida. Se tardaron 9 meses en llegar a este nivel.
Llegados a este punto a los pacientes se les aseguró una ingesta mínima de calcio de 1,5 mg, con suplementos si hacía falta, con el fin de prevenir efectos secundarios a nivel óseo. No se añadieron en ningún momento medicamentos que pudieran influir en el metabolismo del calcio. Entonces se determinaron los dos grupos de pacientes y se empezó a dar el principio activo, así como el placebo en forma de cápsula a ambos grupos aleatoriamente, durante 12 meses.
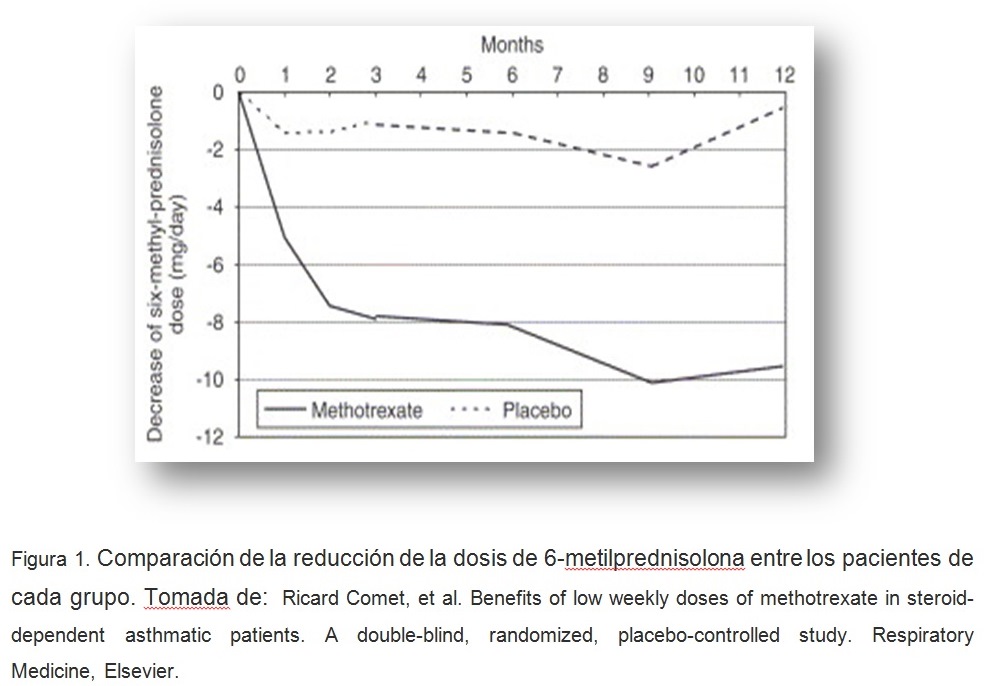 El resultado principal de eficacia fue la disminución de la dosis de esteroides orales. En el grupo tratado con metotrexato la reducción fue significativa, consiguiéndose una reducción de hasta un 54,8% en la dosis de esteroides orales. En el caso del grupo tratado con placebo fue de un 4,4% (figura 1).
El resultado principal de eficacia fue la disminución de la dosis de esteroides orales. En el grupo tratado con metotrexato la reducción fue significativa, consiguiéndose una reducción de hasta un 54,8% en la dosis de esteroides orales. En el caso del grupo tratado con placebo fue de un 4,4% (figura 1).
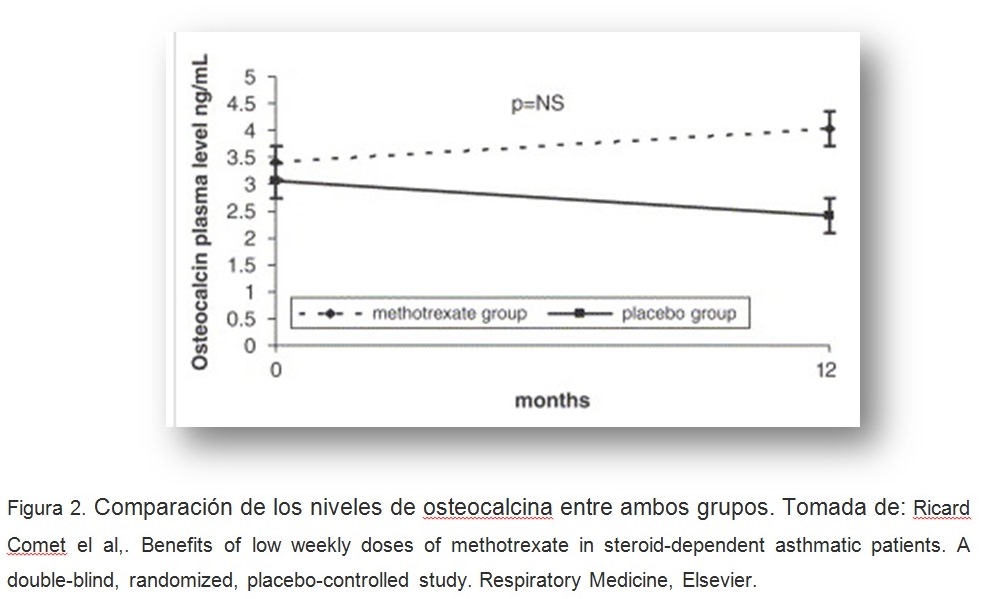 Los resultados secundarios fueron los cambios en el FEV1 y la reducción de la resorción ósea. El resultado de seguridad principal fue estimar la incidencia de los efectos secundarios del fármaco. No se encontró beneficio en cualquiera de los parámetros analizados (densitometría ósea, sangre o análisis de orina) a excepción de una tendencia no estadísticamente significativo de los niveles de osteocalcina a aumentar en el grupo de metotrexato para disminuir en el grupo de placebo (figura 2).
Los resultados secundarios fueron los cambios en el FEV1 y la reducción de la resorción ósea. El resultado de seguridad principal fue estimar la incidencia de los efectos secundarios del fármaco. No se encontró beneficio en cualquiera de los parámetros analizados (densitometría ósea, sangre o análisis de orina) a excepción de una tendencia no estadísticamente significativo de los niveles de osteocalcina a aumentar en el grupo de metotrexato para disminuir en el grupo de placebo (figura 2).
El periodo de estabilización duró una media de 10,3 ± 8,7 meses y la dosis media 6-metilprednisolona en el comienzo de este período fue 20,9 ± 12,4 mg/día. No se encontraron diferencias entre los grupos después de la asignación al azar en términos de duración del período de estabilización o la dosis de esteroides al comienzo. La dosis de 6-metilprednisolona media diaria administrada en el momento de la aleatorización fue: 15,2 ± 8,9 mg/día para toda la población; 17,3 ± 10,1 mg/día para el grupo de metotrexato; 12,8 ± 6,8 mg/día para el grupo placebo. El valor promedio fue de 12 mg/día para ambos grupos.
Los efectos secundarios no fueron importantes. De nuevo, esto se debe probablemente a la baja dosis de metotrexato (sólo dos pacientes abandonaron debido a los efectos secundarios no mortal). No se encontró un aumento significativo de las transaminasas, y los parámetros inmunológicos de los pacientes no se vieron afectados. Llegaron a la conclusión de que esta dosis semanal bajo es lo suficientemente seguro para su uso rutinario.
Conclusión
En conclusión, el metotrexato en dosis semanales bajas demostró ser seguro y útil como agente economizador de esteroides. Los beneficios se producen después de varios meses de tratamiento (más de tres meses) y los beneficios leves para la formación de hueso se pueden asumir. Por lo tanto, a falta de otras alternativas damos por bueno el uso del metotrexato para el tratamiento del asma en aquellos pacientes que tengan preestablecido un régimen de esteroides por vía oral.
Bibliografía
1. R. Polosa, S. Benllinvia, M. Caruso, R. Emma, A. Alamo, M. Leszek Kowalski, C. Domingo. Weekly low-dose methotrexate for reduction of Global Initiative for Asthma Step 5 treatment in severe refractory asthma: study protocol for a randomized controlled trial. BioMed Central. (2014). http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4302097/
2. Ricard Comet, Christian Domingo, Marta Larrosa, Anisi Morón, Montserrat Rué, María José Amengual, Albert Marín. Benefits of low weekly doses of methotrexate in steroid-dependent asthmatic patients. A double-blind, randomized, placebo-controlled study. Respiratory Medicine, Elsevier. (Marzo 2006). http://www.sciencedirect.com/science/article/pii/S0954611105002714
3. B Vrugt, S Wilson, A Bron, J Shute, ST Holgate, R Djukanovic, R Aalbers. Low-dose methotrexate treatment in severe glucocorticoid-dependent asthma: effect on mucosal inflammation and in vitro sensitivity to glucocorticoids of mitogen-induced T-cell proliferation. European Respiratory journal. (Marzo 2000). http://erj.ersjournals.com/content/15/3/478.long
4. S.D. Aaron,R.E. Dales,B. Pham. Management of steroid-dependent asthma with methotrexate: a meta-analysis of randomized clinical trials. Respiratory Medicine, Elsevier. (Agosto 1998). http://www.sciencedirect.com/science/article/pii/S0954611198903559
5. A H Morice, W K Lai. Fatal varicella zoster infection in a severe steroid dependent asthmatic patient receiving methotrexate. Thorax journal. (1995;50:1221-1222). http://thorax.bmj.com/content/50/11/1221.long
6. Gatnash, C. K. Connolly. Fatal chickenpox pneumonia in an asthmatic patient on oral steroids and methotrexate. Thorax journal. (1995;50:422-423). http://thorax.bmj.com/content/50/4/422.long
7. L. M. Kuitert, A. C. Harrison. Pneumocystis carinii pneumonia as a complication of methotrexate treatment of asthma. Thorax journal. (1991; 46:936-937). http://thorax.bmj.com/content/46/12/936.long
8. Todo sobre metotrexato. http://www.todosobremtx.com/Inicio.aspx