De todas las enfermedades descritas desde antiguo, la diabetes es de las pocas que han sobrevivido al examen de la ciencia: desaparecieron el castigo divino, el cólico miserere, los humores, los desequilibrios entre el yin y el yang y tantos otros orígenes de la enfermedad que se consideraban en la Antigüedad. Pero no la diabetes. Ésa era cierta: había y hay algunos pacientes que orinan mucho y dulce, y a ellos, desde el siglo I a.C., se los denomina diabéticos.
La glucosa es muy necesaria para la vida. Nuestro cerebro necesita unos 140 g/día de glucosa: 1 kg a la semana. Y tú, querido lector: ¿te comes esa cantidad de azúcar? No. ¡Ni tú ni nadie! Es tu hígado (90%) y tus riñones (10%) los que lo fabrican a partir de lo que has ingerido. Y si no lo ingieres, lo saca de las reservas. Sí, de los «michelines». Al cerebro no puede faltarle glucosa. Por eso no se escapa ninguna de las calorías ingeridas con la alimentación, y quedan almacenadas como grasas que se podrán convertir en glucosa cuando sea necesario.
El azúcar no es el problema, es la insulina. La falta de insulina hace que la glucosa se acumule en la sangre y no pueda acceder a las reservas (diabetes mellitus tipo 1 [DM1]) o bien que sean las propias reservas las que ya no puedan almacenar más glucosa e impidan el trabajo de la insulina (diabetes mellitus tipo 2 [DM2]). En todo caso, el azúcar se amontona en el torrente sanguíneo y va generando problemas, empezando por los vasos más finos: retinopatías, nefropatías, disfunción eréctil...
En la DM1 falta insulina que lleve la glucosa de las arterias a los órganos. Puede faltar poca, mucha o del todo, depende del estado del páncreas, órgano encargado de producir esta hormona. ¿Todo el páncreas? Bueno, no, sólo una parte de él. El páncreas se encarga de otras tantas tareas que puede seguir realizando aunque no fabrique insulina. Los síntomas aparecen sin previo aviso, pues el fracaso pancreático suele ser repentino.
¿Y por qué el páncreas deja de fabricar insulina? Muy buena pregunta. Si lo supiésemos, se podría poner remedio. Se habla de factores autoinmunes, de predisposición genética, de virus... Puede que sea una mezcla de todo ello. Hay que decir, para tranquilidad de los hijos de diabéticos tipo 1, que el riesgo que tienen de ser ellos mismos diabéticos es sólo un 5% superior al que tiene cualquier hijo de «no diabético».
La terapia en estos pacientes está muy clara: suministrar la insulina que su organismo no produce.
En la DM2 inicialmente no falta insulina, son los depósitos de reservas (el tejido adiposo, la «grasa») los que se resisten a que la insulina haga su trabajo. Al principio, el páncreas incluso fabrica más insulina para vencer esa resistencia, y hay más de la normal en sangre. Con el tiempo también faltará, pues la capacidad del páncreas de secretar insulina se agota. Los síntomas no aparecen hasta que ni siquiera el exceso de insulina en sangre puede vencer la resistencia. Es un proceso lento, largo. ¿Cómo se llega a esta situación, a que el tejido adiposo se defienda de la glucosa? Normalmente por un problema de sobrepeso, de obesidad.
Por eso la primera novedad del 2016 en el tratamiento de la diabetes viene marcada por la recomendación de dejar de usar secretagogos1. Agotan al páncreas, limitan su vida. Es mejor usar terapias que no acorten su funcionalidad: metformina, incretinas, inhibidores del transporte de glucosa ligado al sodio tipo 2 (SGLT2), incluso insulina. Esta recomendación aún no aparece en los consensos, pero es cada vez más frecuente que los investigadores la incluyan en sus artículos.
La recomendación de uso de insulina en pacientes con DM2 es cada vez más frecuente, especialmente en embarazadas, lactantes, periodos pre- y postoperatorios y, en general, en cualquier situación que requiera un control fino de la glucemia. Los límites de tratamiento entre pacientes con DM1 o DM2 se difuminan, pues también a los que padecen diabetes tipo 1 se les recomienda metformina o incretinas asociadas a la insulina. Se trata de hacer un traje a la medida de cada paciente, recurriendo a todo el creciente arsenal terapéutico disponible.
Novedades en farmacoterapia oral: inhibidores del transportador sodio-glucosa tipo 2 (SGLT2)
La unidad funcional del riñón, la nefrona, filtra la sangre para eliminar materiales excedentarios y tóxicos y retener lo útil. De entrada, expulsa casi todo el contenido de la sangre y va recuperando el agua y los elementos necesarios para la vida, dejando fuera del torrente sanguíneo una dilución acuosa llamada «orina». La recuperación de la glucosa hacia el torrente sanguíneo se hace mediante cotransportadores activos de al menos dos tipos (ligados a sodio), estando limitada su capacidad a una presencia de glucosa en sangre no superior a 200 mg/dL. Por encima de esa concentración, deja de reabsorber glucosa, que aparece en la orina, dándole el dulzor que identificaron tanto egipcios como griegos, y que dio pie a los romanos para apellidarla «mellitus» (de miel).
De entre los dos cotransportadores identificados (SGLT1 y SGLT2), el que más influye en la glucosuria es el tipo 2, pues es responsable de la reabsorción del 90% de la glucosa, y sobre éste actúan los nuevos fármacos inhibidores: las «gliflozinas».
Inhibiendo el SGLT2 se consigue eliminar glucosa por la orina de un modo superior al natural; si antes la barrera para desperdiciar un recurso tan importante como la glucosa se situaba en una concentración superior a 200 mg/dL, ahora basta una concentración superior a 160 mg/dL, que muchos diabéticos alcanzan de modo posprandial.
Esa eliminación forzada de la glucosa hace que se reduzca la glucemia, reflejándose en una disminución de la hemoglobina glucosilada de entre medio a un par de puntos porcentuales, más eficaz cuanto peor sea el punto de partida del paciente, independientemente de la insulina y del estado del páncreas. No producen hipoglucemias; si la glucemia no está elevada, no hacen efecto.
Al sacar glucosa de la circulación, se produce una pérdida de peso sostenida a igualdad de ingesta calórica. Además, se fuerza la diuresis, pudiendo colaborar en el control de la presión arterial de modo positivo. Eso, que es una ventaja, supone también un grave inconveniente para muchos, pues aumenta el número de micciones y a su vez la sensación de sed. Es decir, un paciente con DM2 asintomático adquiere los síntomas clásicos de la diabetes: poliuria y polidipsia. La polifagia dependerá de cuánto peso llegue a perder.
Son fármacos sin efecto relevante sobre el perfil lipídico, pero sí están relacionados con una disminución del ácido úrico.
Como efectos secundarios, además de los antes citados, hay que reseñar el incremento de infecciones genitales y urinarias, facilitadas por la continua presencia de glucosa en orina.
Por supuesto, el paciente debe tener una adecuada filtración glomerular (>60) para poder usar estos fármacos (los pacientes que usan diuréticos del asa deben utilizarlos con precaución).
Estos fármacos pueden ser usados por ambos tipos de diabéticos y combinados con cualquier otro tratamiento. En la actualidad, se han comercializado tres: dapagliflozina (Forxiga®), empagliflozina (Jardiance®) y canagliflozina (Invokana®).
Nuevos análogos de incretinas y tres nuevas insulinas
Las siguientes novedades que nos ha traído 2016 vienen por el lado inyectable: dos análogos de incretinas y tres insulinas.
Análogos de incretinas
La palabra incretina es un acrónimo de «INtestinal seCRETion of insulIN», lo cual en castellano directamente suena a incremento, a positivo. Se relaciona con la regulación que se produce a nivel intestinal sobre la producción de insulina y glucagón, mediada por hormonas secretadas en diversos puntos del intestino tras la ingestión de alimento y mientras hay alimento en el tubo digestivo.
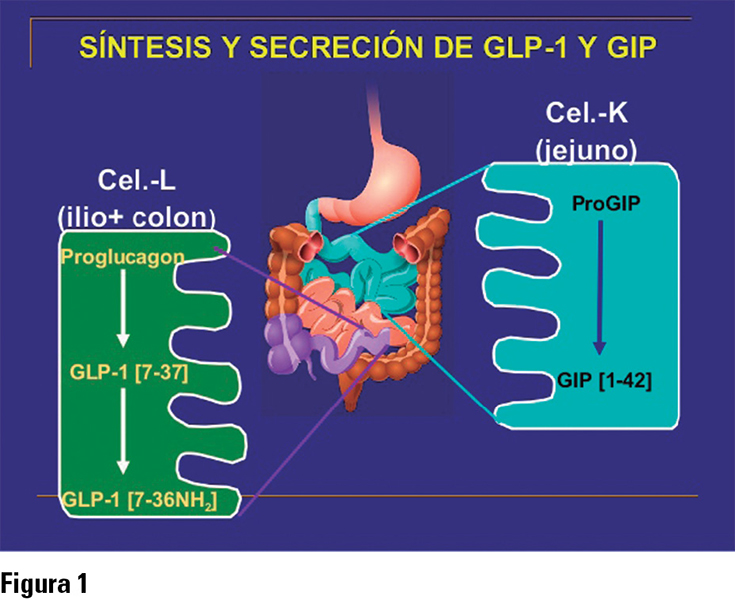 De entre todo el conjunto de hormonas que intervienen, dos son especialmente relevantes: el péptido similar al glucagón (tipo 1, porque hay más [GLP-1]) y el péptido insulinotrópico dependiente de glucosa (GIP). El GIP es producido por las células K que se encuentran en el duodeno y la primera parte del yeyuno, mientras que el GLP-1 se sintetiza por las célula L, que se encuentran principalmente en el íleon y el colon (figura 1). Ambos son secretados en respuesta al consumo de alimentos, sobre todo los ricos en grasas e hidratos de carbono. Tras su liberación, pasan a sangre y se unen a sus receptores específicos antes de ser metabolizados por la enzima dipeptidil peptidasa-4 (DPP-4).
De entre todo el conjunto de hormonas que intervienen, dos son especialmente relevantes: el péptido similar al glucagón (tipo 1, porque hay más [GLP-1]) y el péptido insulinotrópico dependiente de glucosa (GIP). El GIP es producido por las células K que se encuentran en el duodeno y la primera parte del yeyuno, mientras que el GLP-1 se sintetiza por las célula L, que se encuentran principalmente en el íleon y el colon (figura 1). Ambos son secretados en respuesta al consumo de alimentos, sobre todo los ricos en grasas e hidratos de carbono. Tras su liberación, pasan a sangre y se unen a sus receptores específicos antes de ser metabolizados por la enzima dipeptidil peptidasa-4 (DPP-4).
Tanto el GIP como el GLP-1 actúan sobre el páncreas y estimulan la producción de insulina, reduciendo la glucemia.
En los pacientes con DM2 la respuesta a las incretinas suele estar disminuida. Las opciones terapéuticas son dos: inhibir la enzima DPP-4 prolongando la acción incretina natural, o inyectar análogos de incretinas resistentes a DPP-4. ¿Inyectar? Sí, no queda otra opción: son péptidos, y nuestro organismo tiene la sana costumbre de digerir las proteínas que ingerimos. Y esta segunda vía es la que nos trae novedades: albiglutida (Eperzan®) y dulaglutida (Trulicity®), dos análogos de GLP-1 con unas semividas muy largas que permiten cumplir el tratamiento con una inyección semanal.
Aparte de la mejora de la calidad de vida al reducir el número de pinchazos, aportan poco sobre lo ya existente. Frente a la comodidad de un solo uso semanal, hay que reseñar que el dispositivo de inyección de albiglutida es complicado y tedioso. Requiere mucha manipulación por parte del paciente, lo que puede suponer un problema en términos de adherencia al tratamiento. Por el contrario, el dispositivo que han desarrollado para inyectar dulaglutida es portentoso en su sencillez: quitar un precinto, girar menos de un cuarto de vuelta, apoyar contra la zona de inyección y pulsar un botón que extiende la aguja (escondida hasta ese momento), libera el émbolo e inyecta la dosis semanal. Acabado el proceso, la aguja se retrae y sólo queda proceder a desechar el dispositivo.
Como otros análogos del GLP-1, estos fármacos reducen la hemoglobina glucosilada un 0,5-1,2% y ayudan a reducir el peso. Son sinérgicos a otros tratamientos: a metformina, a los inhibidores de SGLT2 e incluso a la insulina.
Insulinas
Y las últimas novedades llegan para los diabéticos de más larga evolución: los de tipo 1 que precisan insulina.
La primera es la nueva insulina degludec (Tresiba®), que fue aprobada por la EMA en febrero de 2013 y ha empezado a comercializarse en España en enero de 2016. Como otras insulinas de ese mismo laboratorio, se ha obtenido en Saccharomyces cerevisiae por tecnología de ADN recombinante.
La principal diferencia con otras insulinas es la duración de su acción, 42 horas, lo cual se estabiliza a partir del tercer día de inyección de la dosis. Eso no supone que se pueda inyectar un día sí y un día no, lo que en mi opinión supondría una clara complicación para la adherencia. No. Una vez inyectada la dosis, se forma un depósito desde el que se absorbe al torrente sanguíneo de forma continuada y lenta, haciendo posible que se adicione la siguiente dosis en cualquier momento entre las 8 y las 42 horas siguientes. Por tanto, aporta «flexibilidad». El diabético se inyecta su dosis el sábado a las 8 a.m., y puede no volver a inyectarse hasta el domingo a las 22 horas sin que se produzcan hiperglucemias.
En su ficha técnica2 se recogen los resultados de distintos estudios que han constatado la reducción significativa de hipoglucemias. Asimismo, incluyen la indicación en pediatría, población para la que será especialmente útil una posología flexible.
Para realizar el cambio de insulina basal, ya sea detemir o glargina, hay que disminuir la dosis un 20%. En mi opinión, va a suponer el mismo avance que supuso glargina (Lantus®) sobre detemir (Levemir®).
Otra novedad es el dispositivo de inyección en que se comercializa: «flextouch», un poco más grueso que los anteriores «flexpen», pues incorpora un mecanismo para que sea un muelle el que, de manera suave y gradual, empuje el émbolo, haciendo menos dolorosa la inyección. Como medida de seguridad, el sonido percibido al incrementar unidades es completamente distinto al de disminuir unidades. Y como detalle de lo mucho que se han esmerado en su diseño, incorpora un pequeño saliente plástico en la «cintura» del dispositivo para impedir que éste ruede por la superficie y se pueda romper por accidente si se cae.
Otra nueva insulina es una glargina biosimilar (Abasaglar®), también conseguida en Escherichia coli, pero por otra vía, pues las empresas productoras de biosimilares no tienen acceso al clon ni a su banco de células original, y tampoco a los procesos de fermentación y purificación originales. Sólo tienen acceso al producto innovador que está comercializado.
Un biosimilar viene a ser un genérico de un medicamento de origen biotecnológico. La patente del original ha expirado, y el biosimilar ha demostrado ser comparable en calidad, eficacia y seguridad al original.
La legislación sobre biosimilares está más desarrollada en Europa gracias a la Agencia Europea del Medicamento (EMA). La Food and Drug Administration (FDA), en cambio, ha admitido muy pocos fármacos biotecnológicos, nombrándolos «genéricos».
La única novedad es que es el primer biosimilar de una insulina disponible en farmacia. Por supuesto, con la legislación española en la mano, no es sustituible ni intercambiable, aunque haya demostrado la misma calidad, eficacia y seguridad.
Y, finalmente, tenemos la insulina glargina «concentrada» (Toujeo®). La unidad de insulina se define como la cantidad necesaria para disminuir la glucemia en ayunas de un conejo de 2 kg, desde 120 hasta 45 mg/dL. Se ha visto que corresponde a la veintidosena parte de un miligramo del producto cristalino puro adoptado como norma. Es decir: 45,4545 (periodo) μg.
Cuando la insulina era porcina y se estableció la unidad, se presentaba en viales de 10 mL, a razón de 40 U/mL. Con el paso del tiempo, se pasó a la insulina de origen humano, refinándola hasta poder presentarla en viales, cartuchos y plumas con 100 U/mL. Cuando pasamos a los análogos de insulina (detemir, glargina), no se cambió la concentración. Ahora se lanza una presentación de glargina en concentraciones de 300 U/mL. Sin mayor novedad. Si se hace el cambio de detemir o glargina a esta nueva concentración de glargina, habrá que incrementar la dosis de inicio en torno a un 20% y luego ajustar según evolución.
Y eso es todo al inicio del año 2016. Se sigue investigando en insulinas de mayor duración, en nuevas dianas terapéuticas, en parches que dispensen la insulina de modo transdérmico, en páncreas artificiales... Atrás queda ya, abandonada en la cuneta de la historia, la insulina inhalada y los trasplantes con células madre totipotenciales.
«Decía Bernardo de Chartres que somos como enanos a los hombros de gigantes. Podemos ver más, y más lejos que ellos, no por la agudeza de nuestra vista ni por la altura de nuestro cuerpo, sino porque somos levantados por su gran altura» (Juan de Salisbury, Metalogicon III, 4. 1159).
«Si he visto más lejos, es porque estoy sentado sobre los hombros de gigantes» (Isaac Newton, en una carta remitida el 15 de febrero de 1676 a Robert Hooke).
Bibliografía
1. Schwartz SS, Epstein S, Corkey BE, Grant SFA, Gavin III JR, Aguilar RB. The time is right for a New Classification System for Diabetes. Rationale and implications of the beta-cell-centric Classification Schema. Diabetes Care. 2016; 39(2): 179-186.
2. Disponible en: http://www.ema.europa.eu/docs/es_ES/document_library/EPAR_-_Product_Information/human/002498/WC500138940.pdf
