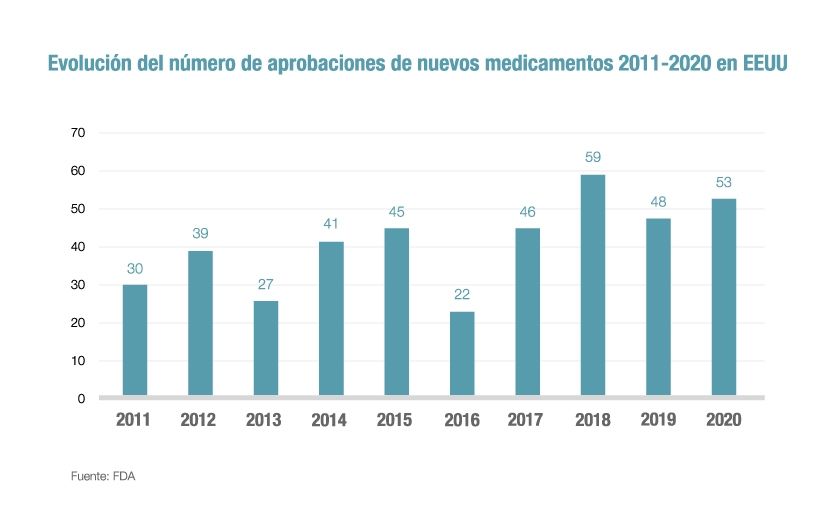
Por otro lado, Food and Drug Administration (FDA), agencia reguladora estadounidense de medicamentos, también ha publicado su informe sobre nuevos medicamentos aprobados en 2020, que supera los resultados recogidos en el documento europeo. De hecho, la FDA aprobó el año pasado 53 nuevos fármacos, un 58% de los cuales han sido identificados como huérfanos, es decir, tratan enfermedades raras o poco frecuentes, y un 40% como first-in-class −medicamentos con mecanismos de acción diferentes a las terapias que ya están en el mercado−, siendo esta la segunda mayor cifra de la última década. Además, dos de cada tres aprobaciones en Estados Unidos se agilizaron por el alto valor de sus aportaciones.
«Más importante que la cantidad de nuevas terapias incluidas en este informe es su valor clínico y las nuevas funciones que estos medicamentos están cumpliendo para mejorar la atención de los pacientes», subraya en el propio documento la directora del Center for Drug Evaluation and Research (CDER), Patricia Cavazzoni.